Cell Death Differ │ 顾建新/汪澜团队揭示凝集素样清道夫受体LOX-1调控肿瘤发生的自噬作用机制
2021年10月5日,复旦大学顾建新/汪澜团队在Cell Death & Differentiation上发表了题为Targeting lectin-like oxidized low-density lipoprotein receptor-1 triggers autophagic program in esophageal cancer的研究成果。该研究发现,凝集素样清道夫受体LOX-1缺失通过启动细胞自噬调控食管癌发生的分子机制。
细胞自噬作为一种细胞内自我消化系统完成自我更新的新陈代谢,通过溶酶体降解其内部受损的细胞器、错误折叠的蛋白质和侵入其内的病原体来维持机体环境稳态。同时,自噬作用的降解产物氨基酸、核苷酸、脂肪酸等可循环利用合成新的大分子和ATP以满足应激条件下细胞和有机体代谢的需要。自噬的这种特点决定了它在肿瘤中的作用复杂而矛盾,不同的环境,包括肿瘤类型、肿瘤发展阶段以及是通过驱动促癌基因还是抑癌基因发挥作用都能影响自噬在肿瘤中的作用。因此,探索自噬在特定肿瘤发生中的具体作用具有重要的临床意义。
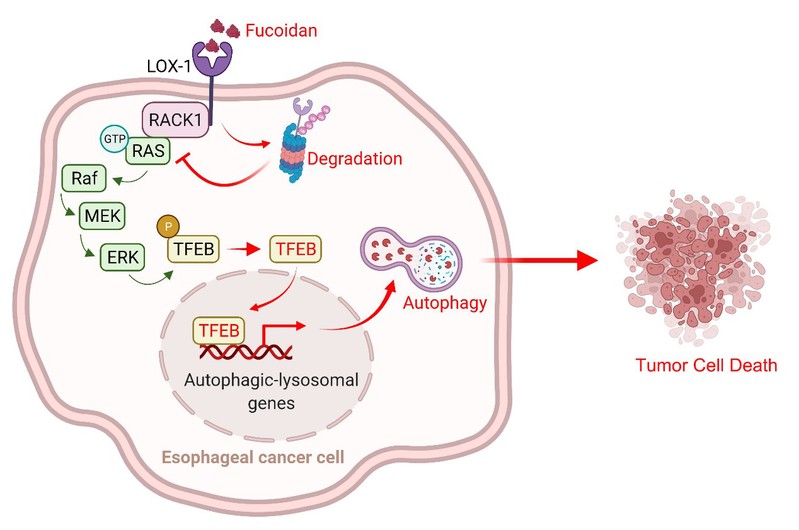
氧化性低密度脂蛋白受体-1(LOX-1)是胞外段含有典型的C型凝集素样结构的模式识别受体,在动脉粥样硬化、高血脂和糖尿病等代谢性疾病中表达上调,而这些代谢性疾病都与肿瘤发生高度相关。该研究发现LOX-1基因缺失通过MAPK/ERK信号机制调控转录因子TFEB启动自噬溶酶体相关基因转录,发挥肿瘤抑制作用。同时发现具有生物活性的岩藻聚糖利用泛素化降解模式降低LOX-1稳定性并诱导肿瘤细胞发生自噬性死亡。本研究阐明糖链结合蛋白凝集素LOX-1在食管癌发生中的自噬调控作用以及效应分子机制,为优化岩藻聚糖的抗肿瘤生物学活性以及食管癌靶向治疗提供理论基础和有效策略。
原文链接:https://www.nature.com/articles/s41418-021-00884-y






